相关题目
4、以K2Cr2O7为基准物采用间接碘法标定0.020mol/L Na2S2O3溶液的浓度。若将消耗的Na2S2O3溶液的体积控制在25mL左右,问应当称取K2Cr2O7多少克?已知:M(K2Cr2O7)=294.2
解:反应式为:
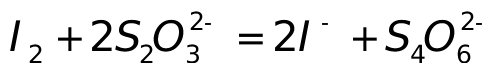
可得计量关系为: 

沉淀滴定法
3、用25.00mL KMnO4溶液恰能氧化一定量的KHC2O4·H2O,而同量KHC2O4 ·H2O又能被20.00mL 0.2000mol/L KOH溶液中和,求KMnO4溶液的浓度。
解:由反应式2MnO4- +5C2O42- +16H+=2Mn2++10CO2+8H2O
可知化学计量关系为:
故 

在酸碱反应中,


2、计算在H2SO4介质中,H+浓度分别为1mol·l-1和0.1 mol·l-1的溶液中VO2+/VO2+电对的条件电极电位(忽略离子强度影响)。已知: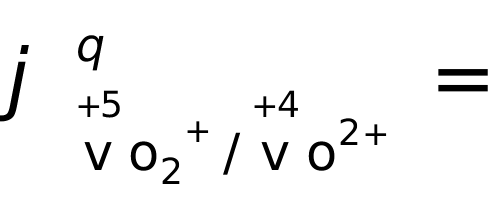 =1.00V。
=1.00V。
解: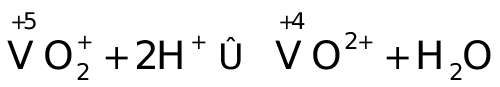
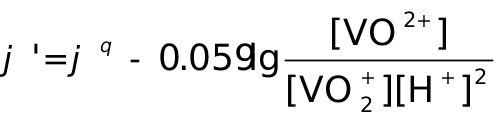
则当[H+]=1mol·l-1时, 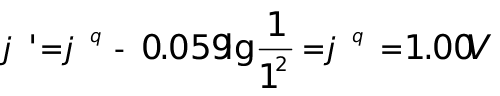
当[H+]=0.1mol·l-1时, 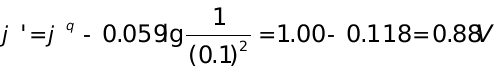
1、计算0.02mol/L KMnO4在1mol/L HClO4溶液中用亚铁盐还原至一半时的电位。已知:在1mol/L HClO4中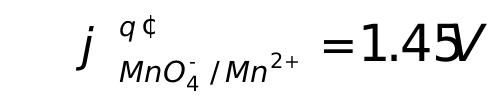 。
。
解:半反应方程为:MnO4 + 8H+ + 5e = Mn2+ + 4H2O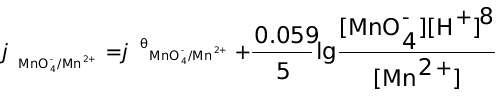

5、某同学如下配制 0.02 mol∙L-1 KMnO4溶液,请指出其错误。
准确称取 1.581g 固体 KMnO4,用煮沸过的蒸馏水溶解,转移至 500 mL 容量瓶,稀释至刻度,然后用干燥的滤纸过滤。
4、用草酸钠标定KMnO4溶液时,温度范围是多少?过高或过低有什么不好?在该实验中能否用HNO3、HCl或HAc来调节溶液的酸度?为什么? 催化剂和指示剂又是什么?
3、简述硫代硫酸钠标准溶液的配制与标定所用基准物、反应的方程式、温度、酸度、滴定速度、所用指示剂及滴加时机。
2、请回答 K2Cr2O7 标定 Na2S2O3时实验中的有关问题。
(1) 为何不采用直接法标定,而采用间接碘量法标定?
(2) Cr2O72-氧化 I-反应为何要加酸,并加盖在暗处放置 5 min,而用Na2S2O3 滴定前又要加蒸馏水稀释?
1、简述高锰酸钾标准溶液的配制;标定所用基准物;反应的方程式;温度;酸度;滴定速度;催化剂及所用指示剂。
13、( )氧化还原滴定反应其化学计量点电势与两电对的条件电势和试剂的浓度有关。




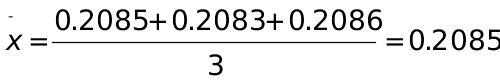 (mol∙L-1)
(mol∙L-1)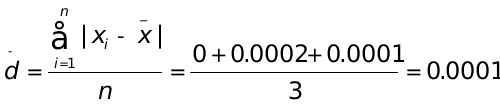 (mol∙L-1)
(mol∙L-1)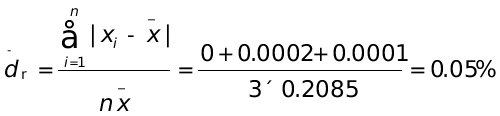
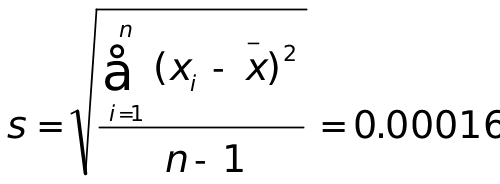 (mol∙L-1)
(mol∙L-1)






