相关题目
4、以下银量法需采用返滴定方式测定的是( )。
3、以铁铵矾为指示剂,用返滴定法以NH4SCN标准溶液滴定Clˉ时,下列错误的是( )。
2、莫尔( )法测定Clˉ含量时,要求介质在pH=6.5~10.0范围内,若酸度过高,则会( )。
1、关于以K2CrO4为指示剂的莫尔( )法,下列说法正确的是( )。
4、以K2Cr2O7为基准物采用间接碘法标定0.020mol/L Na2S2O3溶液的浓度。若将消耗的Na2S2O3溶液的体积控制在25mL左右,问应当称取K2Cr2O7多少克?已知:M(K2Cr2O7)=294.2
解:反应式为:
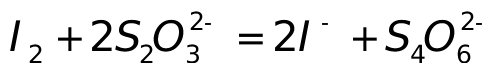
可得计量关系为: 

沉淀滴定法
3、用25.00mL KMnO4溶液恰能氧化一定量的KHC2O4·H2O,而同量KHC2O4 ·H2O又能被20.00mL 0.2000mol/L KOH溶液中和,求KMnO4溶液的浓度。
解:由反应式2MnO4- +5C2O42- +16H+=2Mn2++10CO2+8H2O
可知化学计量关系为:
故 

在酸碱反应中,


2、计算在H2SO4介质中,H+浓度分别为1mol·l-1和0.1 mol·l-1的溶液中VO2+/VO2+电对的条件电极电位(忽略离子强度影响)。已知: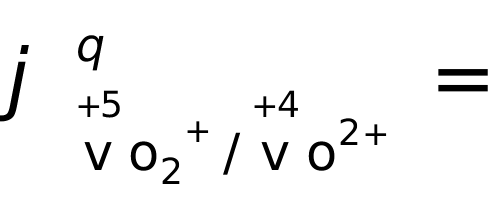 =1.00V。
=1.00V。
解: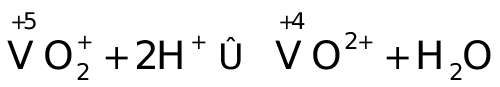
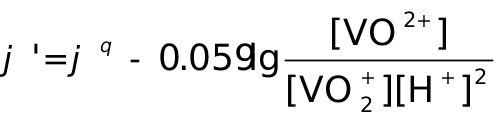
则当[H+]=1mol·l-1时, 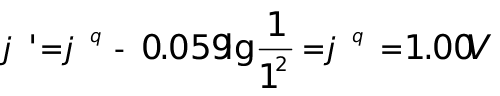
当[H+]=0.1mol·l-1时, 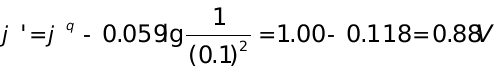
1、计算0.02mol/L KMnO4在1mol/L HClO4溶液中用亚铁盐还原至一半时的电位。已知:在1mol/L HClO4中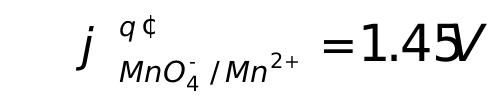 。
。
解:半反应方程为:MnO4 + 8H+ + 5e = Mn2+ + 4H2O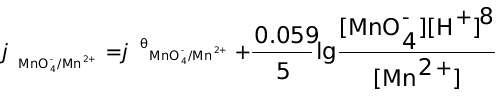

5、某同学如下配制 0.02 mol∙L-1 KMnO4溶液,请指出其错误。
准确称取 1.581g 固体 KMnO4,用煮沸过的蒸馏水溶解,转移至 500 mL 容量瓶,稀释至刻度,然后用干燥的滤纸过滤。
4、用草酸钠标定KMnO4溶液时,温度范围是多少?过高或过低有什么不好?在该实验中能否用HNO3、HCl或HAc来调节溶液的酸度?为什么? 催化剂和指示剂又是什么?










