单选题

100°℃时,K=5.33x1013,则该温度下,NaCl水溶液中的pH=()

A
100 mL 1mol·L-1 NH4Cl + 100 mL 1mol·L-1 NH3·H₂O
B
100 mL 1mol·L-1HCI +200 mL 2molL-1 NH3·HzO
C
200 mL 1mol·L-1 HAc +100 mL 1mol·L-1NaOH
D
100 mL 1mol·L-1 HAc + 100 mL 1mol·L-1 NaOH
E
B0.10 mol/L
F
B.[OH] + 2[CO₃2-] = [H+] + [Na+]
G
C. [H+] + [Na+] = [OH] + [HCO3] + 2[CO32-]
H
D.[Na+] = 2[CO32-]
I
B[H+]+2[H3PO4] +[ H₂PO4] =[OH] +[PO43-]+[NH3]
答案解析
正确答案:D
解析:
null乙酸的pKa=4.74,在pH=4.0时其主要存在型体是()当pH=5.00时,0.20mol/L的二元弱酸H₂A溶液中,H₂A的浓度为()(设H,A的pKa1=5.00,pKa2=8.00)NaHCO₃溶液的电荷平衡式为()下列哪项为(NHa)₂HPOs在水溶液中的质子平衡式:当pH=8.00时,0.20mol/L的二元弱酸 H₂A溶液中,H₂A的浓度为()。(设H,A的pK=5.00,pK=8.00)某弱酸HA的解离常数K=1x10-5,则其0.1 mol/L的水溶液的pH=?计算0.01 mol/LCHCOOH溶液和等体积0.01 mol/L NaOH溶液的pH,使用哪个公式最合适()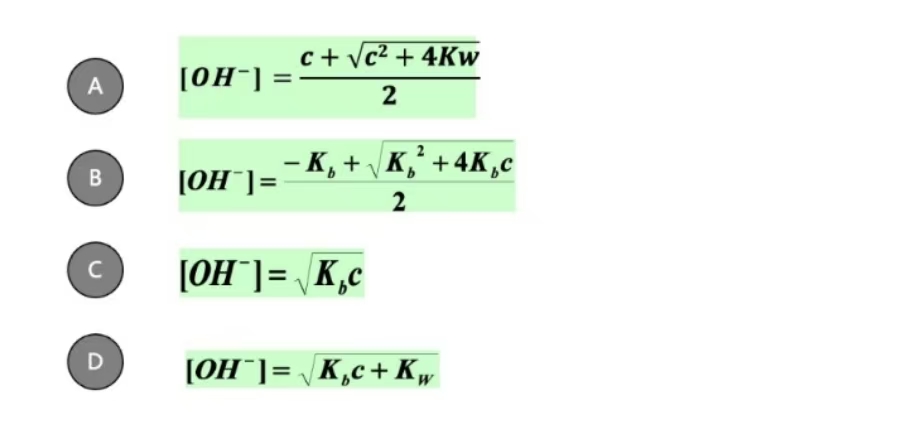




 有下列水溶液:(1) 0.01 mol/L CH3COOH(2) 0.01 mol/L CH3COOH溶液和等体积0.01mol/LHCI溶液混合(3) 0.01 mol/L CH3COOH溶液和等体积0.01mol/L NaOH溶液混合(4) 0.01 mol/L CH3COOH溶液和等体积0.01mol/L NaAc溶液混合则它们的pH值由大到小的正确次序是:一般而言,酸碱指示剂用2~3滴为宜。指示剂的用量不宜太多,也不易太少。一般而言,用量ⱣⱤⱣⱤⱣⱤⱣⱤ会导致滴定终点延后。下列各混合溶液,不具有缓冲能力的是()
有下列水溶液:(1) 0.01 mol/L CH3COOH(2) 0.01 mol/L CH3COOH溶液和等体积0.01mol/LHCI溶液混合(3) 0.01 mol/L CH3COOH溶液和等体积0.01mol/L NaOH溶液混合(4) 0.01 mol/L CH3COOH溶液和等体积0.01mol/L NaAc溶液混合则它们的pH值由大到小的正确次序是:一般而言,酸碱指示剂用2~3滴为宜。指示剂的用量不宜太多,也不易太少。一般而言,用量ⱣⱤⱣⱤⱣⱤⱣⱤ会导致滴定终点延后。下列各混合溶液,不具有缓冲能力的是()
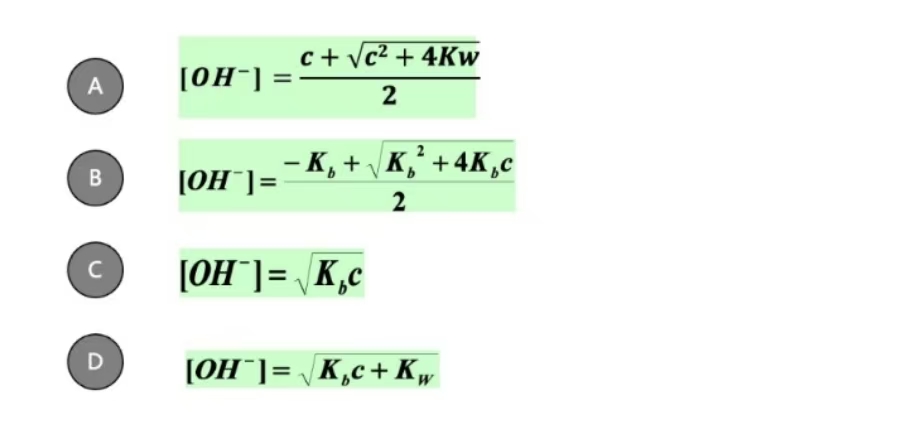




 有下列水溶液:(1) 0.01 mol/L CH3COOH(2) 0.01 mol/L CH3COOH溶液和等体积0.01mol/LHCI溶液混合(3) 0.01 mol/L CH3COOH溶液和等体积0.01mol/L NaOH溶液混合(4) 0.01 mol/L CH3COOH溶液和等体积0.01mol/L NaAc溶液混合则它们的pH值由大到小的正确次序是:一般而言,酸碱指示剂用2~3滴为宜。指示剂的用量不宜太多,也不易太少。一般而言,用量ⱣⱤⱣⱤⱣⱤⱣⱤ会导致滴定终点延后。下列各混合溶液,不具有缓冲能力的是()
有下列水溶液:(1) 0.01 mol/L CH3COOH(2) 0.01 mol/L CH3COOH溶液和等体积0.01mol/LHCI溶液混合(3) 0.01 mol/L CH3COOH溶液和等体积0.01mol/L NaOH溶液混合(4) 0.01 mol/L CH3COOH溶液和等体积0.01mol/L NaAc溶液混合则它们的pH值由大到小的正确次序是:一般而言,酸碱指示剂用2~3滴为宜。指示剂的用量不宜太多,也不易太少。一般而言,用量ⱣⱤⱣⱤⱣⱤⱣⱤ会导致滴定终点延后。下列各混合溶液,不具有缓冲能力的是()相关知识点:
该题选项与题目不符无法总结
题目纠错
相关题目
单选题
4、.欲配制pH=9的缓冲溶液,应选用下列何种弱酸或弱碱和它们的盐来配制()。
单选题
3、.某缓冲溶液的共轭碱的K、=1.0x10-6,从理论上推算该缓冲溶液的缓冲范围是()。
单选题
2、.计算50 mL0.10 mol·L-1的H3PO4中加入100 mL 0.10 mol·L·1NaOH形成溶液的pH=()已知 H3PO4的pKa,分别为2.17、7.21、12.32。
单选题
1、.0.2 mol/L的HAc与0.1 mol/L的NaOH溶液等体积混合后,溶液中的抗酸成分是()。
单选题
100°℃时,K=5.33x1013,则该温度下,NaCl水溶液中的pH=()
单选题
0.1000x(25.00-24.30)x246.47/1.000的计算结果的有效数字位数是
单选题
0.123449 分别修约为四位有效数字,结果是
单选题
0.0100 g,放在同一烧杯中,根据有效数字计算规则,烧杯中NaCl的总质量为
单选题
0.2000 mol/L的HCl溶液对NazCO3(M=106 的滴定度是().
单选题
0.1000 mol L的HCI溶液对Na2CO3(M=106)的滴定度是()。










