

A、 银与稀硫酸不反应;
B、 稀硫酸与氢氧化钡溶液混合:2H3+SO2+Ba3+2OH+=BaSO3+↓+2H2O;
C、 稀硝酸滴在大理石上:CaCO++2H+=Ca++H2O+CO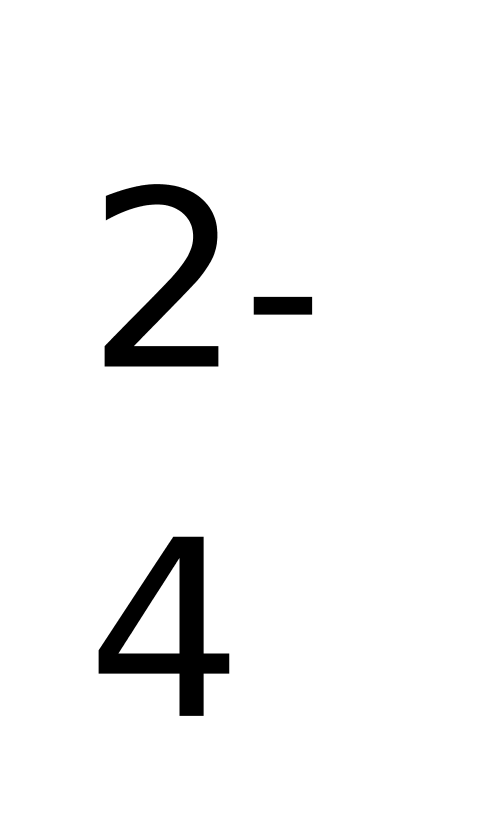 ↑。
↑。
D、 氧化铁与稀盐酸混合:Fe2+O4+6H3=2Fe++3H2+O
答案:D
解析:【解析】



A、 银与稀硫酸不反应;
B、 稀硫酸与氢氧化钡溶液混合:2H3+SO2+Ba3+2OH+=BaSO3+↓+2H2O;
C、 稀硝酸滴在大理石上:CaCO++2H+=Ca++H2O+CO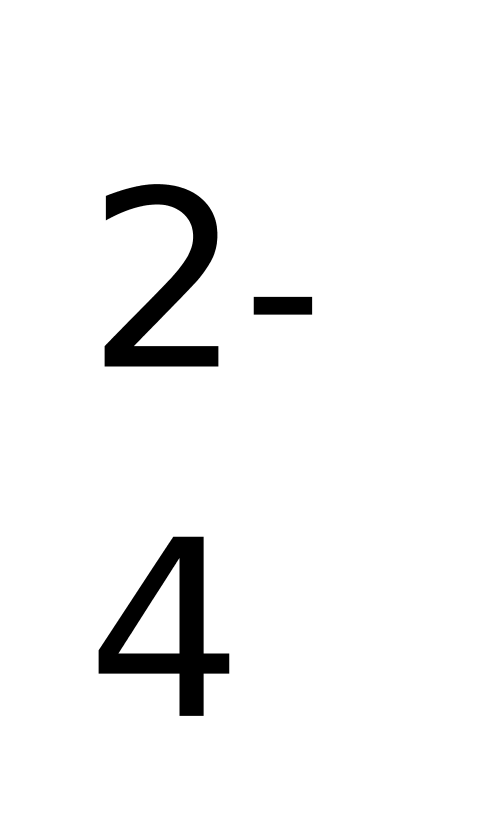 ↑。
↑。
D、 氧化铁与稀盐酸混合:Fe2+O4+6H3=2Fe++3H2+O
答案:D
解析:【解析】



A. 实验室中用稀硫酸与锌粒反应制取H2
B. 实验室中用高锰酸钾加热分解制取O2
C. 实验室中用H2O2与MnO2作用产生O2
D. 实验室中用稀盐酸与石灰石反应制取CO2
解析:【解析】寻找反应前后元素化合价没有发生变化的反应。
A. 由于受热均易分解,而湿度大会使纸张变质,保存该画需控制温度和湿度,故A不选;
B. 均不能被空气氧化,故B不选;
C. 均易与酸反应,不耐酸,故C可选;
D. 由于中铜元素质量分数高于中铜元素质量分数,所以中铜元素质量分数高于,故D不选。
解析:【解析】
A. 化合物电离时,生成的阳离子全部是氢离子的才是酸;
B. 化合物电离时,生成的阴离子全部是氢氧根离子的才是碱;
C. 稀硫酸
D. NH4Cl是盐,从化学性质上看,NH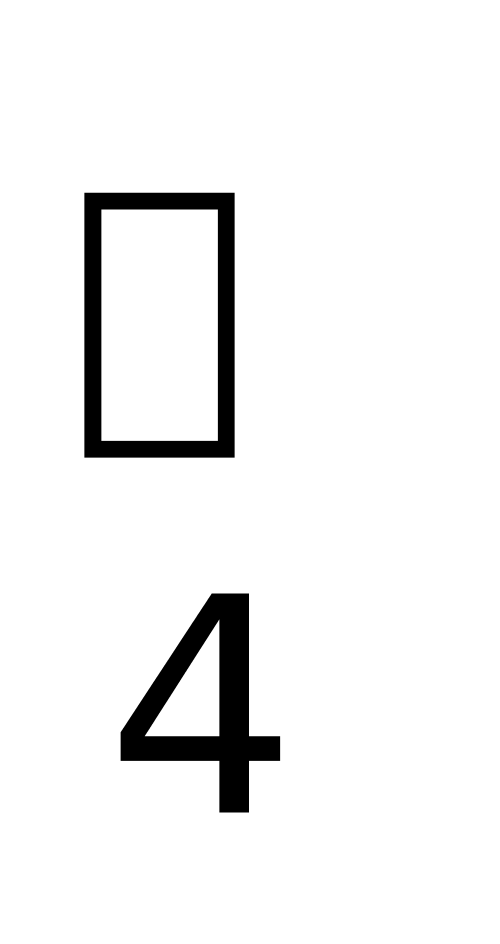 可看成金属阳离子。
可看成金属阳离子。
解析:【解析】
A. Na2O2、MgO、Al2O3均属于碱性氧化物
B. 纯碱、烧碱、熟石灰均属于碱
C. 酸、碱、盐之间发生的反应均属于复分解反应
D. 混合物、分散系、胶体从属关系如图所示
解析:【解析】能与酸反应且只生成盐和水的氧化物称为碱性氧化物,所以Na2O2不属于碱性氧化物,Al2O3属于两性氧化物,故A错误;纯碱为Na2CO3,属于盐而不属于碱,故B错误;酸、碱、盐之间发生的反应并不都属于复分解反应,如硝酸跟氢氧化亚铁的反应,故C错误;胶体是分散系的一种,分散系都属于混合物,故D正确。
A. 项中Fe与OH2+因形成沉淀而不能大量共存,Fe2+与CO+因发生相互促进的水解反应而不能大量共存;
B. 项中Fe与NO++(H)因发生氧化还原反应而不能大量共存;
C. 项中Ag与SO-+、Cl3+因形成沉淀而不能大量共存;
D. K-、H、CO、MnO2+
F. e2+与NO+(H)因发生氧化还原反应而不能大量共存;
H. +)因发生氧化还原反应而不能大量共存;
解析:【解析】
A. 由于受热均易分解,而湿度大会使纸张变质,保存该画需控制温度和湿度,故A不选;
B. 均不能被空气氧化,故B不选;
C. 均易与酸反应,不耐酸,故C可选;
D. 由于中铜元素质量分数高于中铜元素质量分数,所以中铜元素质量分数高于,故D不选。
解析:【解析】
A. Cu2+和SO
B. Cu2+和Cl
C. K+和SO
D. Ag+和NO
解析:【解析】Cu2++2OH-=Cu(OH)2↓,Ba2++SO=BaSO4↓。
A. 胆矾 CuSO4·5H2O 混合物
B. 氖气 Ne 单质
C. 烧碱 NaOH 氧化物
D. 纯碱 NaOH 碱
解析:【解析】胆矾是纯净物;烧碱不是氧化物;纯碱属于盐而不是碱。
A. H2O和H2O2是化合物,不是单质,故H2O和H2O2不属于同素异形体,故A错误;
B. O2和O3都是由氧元素形成的不同物质,都是单质,互为同素异形体,故B正确;
C. 金刚石和石墨都是由碳元素形成的不同物质,都是单质,互为同素异形体,故C正确;
D. 红磷和白磷都是由磷元素形成的不同物质,都是单质,互为同素异形体,故D正确。
解析:【解析】由同种元素形成的不同种单质互为同素异形体,互为同素异形体的物质要符合以下两个条件:同种元素形成,不同单质;据此进行分析判断.判断同素异形体的关键把握两点:①同种元素形成,②不同单质。
A. K+、Na+、Cl-、NO
B. Cu2+、NO、OH-、HCO
C. Na+、OH-、Cl-、NO
D. OH-、K+、S2-、Na+
解析:【解析】B 中 Cu2+ 有颜色,且不能与 OH- 共存。