

A、 三氧化硫的水溶液能导电,所以三氧化硫是电解质
B、 自由移动离子数目多的电解质溶液导电能力一定强
C、 NaHSO4在水溶液及熔融状态下均可电离出Na+、H+、SO
D、 NH3是非电解质,但其水溶液能导电
答案:D
解析:【解析】三氧化硫本身不能电离出离子,是非电解质,A错误;离子数目多的溶液中,离子浓度不一定大,离子所带电荷数不一定多,其导电能力不一定强,B错误;NaHSO4在熔融状态下只能电离出Na+、HSO,C错误;NH3是非电解质,但其溶于水后可形成电解质NH3·H2O,溶液能导电,D正确。



A、 三氧化硫的水溶液能导电,所以三氧化硫是电解质
B、 自由移动离子数目多的电解质溶液导电能力一定强
C、 NaHSO4在水溶液及熔融状态下均可电离出Na+、H+、SO
D、 NH3是非电解质,但其水溶液能导电
答案:D
解析:【解析】三氧化硫本身不能电离出离子,是非电解质,A错误;离子数目多的溶液中,离子浓度不一定大,离子所带电荷数不一定多,其导电能力不一定强,B错误;NaHSO4在熔融状态下只能电离出Na+、HSO,C错误;NH3是非电解质,但其溶于水后可形成电解质NH3·H2O,溶液能导电,D正确。



A. 三氧化硫的水溶液能导电,所以三氧化硫是电解质
B. 自由移动离子数目多的电解质溶液导电能力一定强
C. NaHSO4在水溶液及熔融状态下均可电离出Na+、H+、SO
D. NH3是非电解质,但其水溶液能导电
解析:【解析】离子数目多的溶液中,离子浓度不一定大,离子所带电荷数不一定多,其导电能力不一定强,B错误;NaHSO4在熔融状态下只能电离出Na+、HSO,C错误;NH3是非电解质,但其溶于水后可形成电解质NH3·H2O,溶液能导电,D。
A. 由于受热均易分解,而湿度大会使纸张变质,保存该画需控制温度和湿度,故A不选;
B. 均不能被空气氧化,故B不选;
C. 均易与酸反应,不耐酸,故C可选;
D. 由于中铜元素质量分数高于中铜元素质量分数,所以中铜元素质量分数高于,故D不选。
解析:【解析】
A. ①②③④
B. ②③④
C. ①③④
D. ①②③
解析:【解析】①铜与氧气反应生成氧化铜,氧化铜与硫酸反应生成硫酸铜,硫酸铜与硝酸钡反应生成硝酸铜,铜和浓硫酸反应可生成硫酸铜,再利用较活泼金属与不活泼金属的盐溶液发生的置换反应可实现丙→甲、丁→甲的反应,故①能实现转化。②碳酸钠和氢氧化钙反应生成氢氧化钠,氢氧化钠和二氧化碳反应生成碳酸氢钠,碳酸氢钠分解或与盐酸反应生成二氧化碳,二氧化碳与氢氧化钠能反应生成碳酸钠,碳酸钠与二氧化碳反应生成碳酸氢钠,碳酸氢钠与氢氧化钠反应生成碳酸钠,故②能实现转化。③(NH4)2SO3和氯化钙反应生成亚硫酸钙沉淀,亚硫酸钙和盐酸反应生成二氧化硫,过量的二氧化硫和一水合氨反应生成亚硫酸氢铵,故③能实现转化。④Fe与水蒸气在高温下反应生成Fe3O4,Fe3O4被还原可生成FeO,FeO可与盐酸反应生成FeCl2,FeCl2可被置换生成Fe,Fe在高温下与氧气反应生成FeO,FeO可与CO反应生成Fe,故④能实现转化。
A. 化合物电离时,生成的阳离子全部是氢离子的才是酸;
B. 化合物电离时,生成的阴离子全部是氢氧根离子的才是碱;
C. 稀硫酸
D. NH4Cl是盐,从化学性质上看,NH可看成金属阳离子。
解析:【解析】
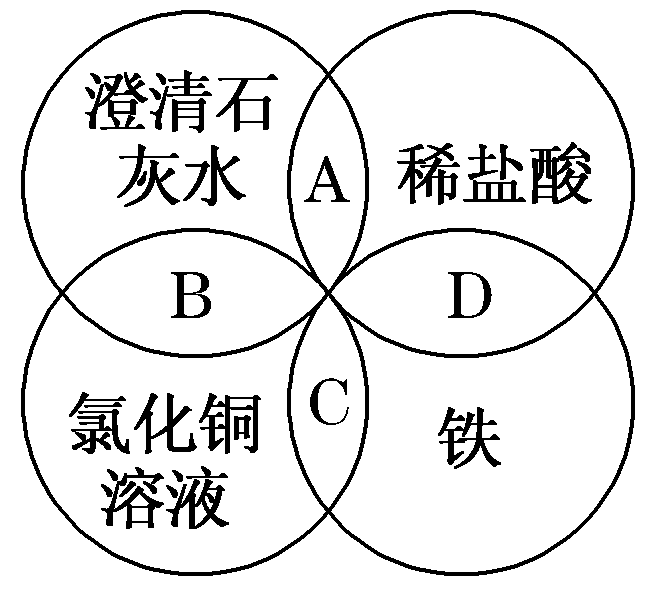
A. 项正确的离子方程式为OH-+H+===H2O;
B. 项正确的离子方程式为
C. u2++2OH-===Cu(OH)2↓;
D. 项正确的离子方程式为Fe+2H+===Fe2++H2↑。
F. e+2H+===Fe2++H2↑。
H. +===Fe2++H2↑。
解析:【解析】
A. 银与稀硫酸不反应;
B. 稀硫酸与氢氧化钡溶液混合:2H++SO+Ba2++2OH-=BaSO4↓+2H2O;
C. 稀硝酸滴在大理石上:CaCO3+2H+=Ca2++H2O+CO2↑。
D. 氧化铁与稀盐酸混合:Fe2O3+6H+=2Fe3++3H2O
解析:【解析】
A. H2O和H2O2是化合物,不是单质,故H2O和H2O2不属于同素异形体,故A错误;
B. O2和O3都是由氧元素形成的不同物质,都是单质,互为同素异形体,故B正确;
C. 金刚石和石墨都是由碳元素形成的不同物质,都是单质,互为同素异形体,故C正确;
D. 红磷和白磷都是由磷元素形成的不同物质,都是单质,互为同素异形体,故D正确。
解析:【解析】由同种元素形成的不同种单质互为同素异形体,互为同素异形体的物质要符合以下两个条件:同种元素形成,不同单质;据此进行分析判断.判断同素异形体的关键把握两点:①同种元素形成,②不同单质。
 (2)水是人体的重要组成部分,是人体中含量最多的一种物质。而“四种基本反应类型与氧化还原反应的关系”可用下图表达。
(2)水是人体的重要组成部分,是人体中含量最多的一种物质。而“四种基本反应类型与氧化还原反应的关系”可用下图表达。 试写出有水参加的符合反应类型Ⅳ的一个化学方程式:( ),其中水为( )剂。(3)过氧化氢俗称双氧水,医疗上利用它的杀菌消毒作用来清洗伤口。H2O2有时可作为矿业废液消毒剂,有“绿色氧化剂”的美称;如消除采矿业胶液中的氰化物(如KCN),可经以下反应实现:KCN+H2O2+H2O ===A+NH3↑,试写出生成物A的化学式:( ),并阐明H2O2被称为绿色氧化剂的理由:( )。(4)氯化铵常用于焊接。如:在焊接铜器时用氯化铵除去铜器表面的氧化铜以便焊接,其反应为( )CuO+( )NH4Cl( )Cu+( )CuCl2+( )N2↑+( )H2O。①配平此氧化还原反应方程式。②该反应中,被氧化的元素是( )(填元素名称),氧化剂是( )(填化学式)。
试写出有水参加的符合反应类型Ⅳ的一个化学方程式:( ),其中水为( )剂。(3)过氧化氢俗称双氧水,医疗上利用它的杀菌消毒作用来清洗伤口。H2O2有时可作为矿业废液消毒剂,有“绿色氧化剂”的美称;如消除采矿业胶液中的氰化物(如KCN),可经以下反应实现:KCN+H2O2+H2O ===A+NH3↑,试写出生成物A的化学式:( ),并阐明H2O2被称为绿色氧化剂的理由:( )。(4)氯化铵常用于焊接。如:在焊接铜器时用氯化铵除去铜器表面的氧化铜以便焊接,其反应为( )CuO+( )NH4Cl( )Cu+( )CuCl2+( )N2↑+( )H2O。①配平此氧化还原反应方程式。②该反应中,被氧化的元素是( )(填元素名称),氧化剂是( )(填化学式)。
解析:【解析】(1)煤的形成发生复杂的物理化学变化,C元素的化合价一定变化,为氧化还原反应,A项错误;太阳能电池工作是太阳能转化为电能的原电池装置,是化学变化,B项错误;简单机械织布,为物理变化,C项正确;烧制陶瓷发生复杂的物理化学变化,存在氧化过程,涉及氧化还原反应,如涉及碳的燃烧等,D项错误。(2)由图可知,Ⅳ为氧化还原反应,且属于置换反应,如2Na+2H2O ===2NaOH+H2↑,水中H元素的化合价降低,则水为氧化剂。(3)由反应KCN+H2O2+H2O === A+NH3↑遵循元素、原子守恒可知,生成物A应该是KHCO3;双氧水作氧化剂,还原产物是水,环保无污染,同时不会向溶液中引入杂质离子,故H2O2被称为绿色氧化剂。(4)①Cu元素的化合价由+2价降低为0价,N元素的化合价由-3价升高为0价,由电子守恒、原子守恒可知,NH4Cl失去3个电子,而Cu得到2个电子,根据得失电子守恒,NH4Cl的化学计量数为2,铜的化学计量数为3,再结合原子守恒可知,化学方程式为4CuO+2NH4Cl === 3Cu+CuCl2+N2+4H2O;②N元素失去电子被氧化,Cu元素得到电子被还原,则CuO为氧化剂。