

A、 化合物电离时,生成的阳离子全部是氢离子的才是酸;
B、 化合物电离时,生成的阴离子全部是氢氧根离子的才是碱;
C、 稀硫酸
D、 NH4Cl是盐,从化学性质上看,NH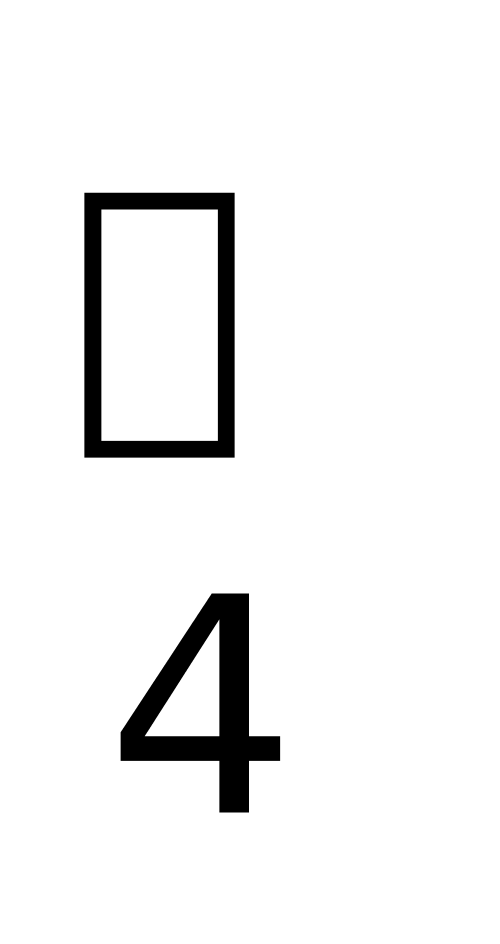 可看成金属阳离子。
可看成金属阳离子。
答案:C
解析:【解析】



A、 化合物电离时,生成的阳离子全部是氢离子的才是酸;
B、 化合物电离时,生成的阴离子全部是氢氧根离子的才是碱;
C、 稀硫酸
D、 NH4Cl是盐,从化学性质上看,NH 可看成金属阳离子。
可看成金属阳离子。
答案:C
解析:【解析】



A. 项正确的离子方程式为OH-+H+===H2O;
B. 项正确的离子方程式为
C. u2++2OH-===Cu(OH)2↓;
D. 项正确的离子方程式为Fe+2H+===Fe2++H2↑。
F. e+2H+===Fe2++H2↑。
H. +===Fe2++H2↑。
解析:【解析】
A. 实验室中用稀硫酸与锌粒反应制取H2
B. 实验室中用高锰酸钾加热分解制取O2
C. 实验室中用H2O2与MnO2作用产生O2
D. 实验室中用稀盐酸与石灰石反应制取CO2
解析:【解析】寻找反应前后元素化合价没有发生变化的反应。
A. Na2O2、MgO、Al2O3均属于碱性氧化物
B. 纯碱、烧碱、熟石灰均属于碱
C. 酸、碱、盐之间发生的反应均属于复分解反应
D. 混合物、分散系、胶体从属关系如图所示
解析:【解析】能与酸反应且只生成盐和水的氧化物称为碱性氧化物,所以Na2O2不属于碱性氧化物,Al2O3属于两性氧化物,故A错误;纯碱为Na2CO3,属于盐而不属于碱,故B错误;酸、碱、盐之间发生的反应并不都属于复分解反应,如硝酸跟氢氧化亚铁的反应,故C错误;胶体是分散系的一种,分散系都属于混合物,故D正确。
A. Cu2+和SO
B. Cu2+和Cl
C. K+和SO
D. Ag+和NO
解析:【解析】Cu2++2OH-=Cu(OH)2↓,Ba2++SO=BaSO4↓。
A. K+、Na+、Cl-、NO
B. Cu2+、NO、OH-、HCO
C. Na+、OH-、Cl-、NO
D. OH-、K+、S2-、Na+
解析:【解析】B 中 Cu2+ 有颜色,且不能与 OH- 共存。
A. K-、Na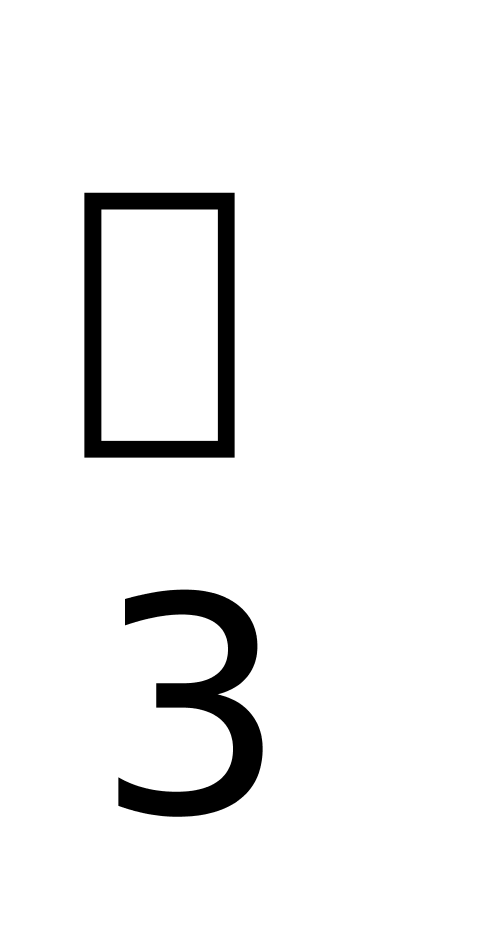 、Cl+、NO2+ - ++-
、Cl+、NO2+ - ++-
B. Cu、NO、OH、HCO
C. Na、OH2+、Cl 、NO-
、NO- +2+ - +
+2+ - +
D. OH+、K-、S 、Na
、Na
解析:【解析】B 中 Cu2+ 有颜色,且不能与 OH- 共存。
A. I3+的还原性强于Fe
B. I-的氧化性强于Fe2
C. ③易发生的主要原因是Fe(OH)2+比Fe(OH)3+更难溶
D. 溶液酸碱性对Fe2+和Fe2的氧化性或还原性没有影响
解析:【解析】由①可知还原性:I->Fe2+,由②可知还原性:Fe>Fe2+,无法判断I-和Fe的还原性强弱,A项错误;由①可知氧化性:Fe3+>I2,B项错误;由③可知,碱性条件下I3+能将Fe(OH)-氧化为Fe(OH)2,所以溶液酸碱性对Fe2+和Fe3+的氧化性或还原性有影响,D项错误。
A. 项中Fe与OH2+因形成沉淀而不能大量共存,Fe2+与CO+因发生相互促进的水解反应而不能大量共存;
B. 项中Fe与NO++(H)因发生氧化还原反应而不能大量共存;
C. 项中Ag与SO-+、Cl3+因形成沉淀而不能大量共存;
D. K-、H、CO、MnO2+
F. e2+与NO+(H)因发生氧化还原反应而不能大量共存;
H. +)因发生氧化还原反应而不能大量共存;
解析:【解析】
A. 氧化性
B. 还原性
C. 碱性
D. 酸性
解析:【解析】维生素C可防止Fe2+变为Fe3+,所以维生素C能将Fe3+还原为Fe2+,则维生素C具有还原性。