

A、 项中Fe3+与OH-因形成沉淀而不能大量共存,Fe3+与CO因发生相互促进的水解反应而不能大量共存;
B、 项中Fe2+与NO(H+)因发生氧化还原反应而不能大量共存;
C、 项中Ag+与SO、Cl-因形成沉淀而不能大量共存;
D、 K+、H+、CO、MnO
F、 e2+与NO(H+)因发生氧化还原反应而不能大量共存;
H、 +)因发生氧化还原反应而不能大量共存;
答案:B
解析:【解析】



A、 项中Fe3+与OH-因形成沉淀而不能大量共存,Fe3+与CO因发生相互促进的水解反应而不能大量共存;
B、 项中Fe2+与NO(H+)因发生氧化还原反应而不能大量共存;
C、 项中Ag+与SO、Cl-因形成沉淀而不能大量共存;
D、 K+、H+、CO、MnO
F、 e2+与NO(H+)因发生氧化还原反应而不能大量共存;
H、 +)因发生氧化还原反应而不能大量共存;
答案:B
解析:【解析】



A. 项中Fe与OH2+因形成沉淀而不能大量共存,Fe2+与CO+因发生相互促进的水解反应而不能大量共存;
B. 项中Fe与NO++(H)因发生氧化还原反应而不能大量共存;
C. 项中Ag与SO-+、Cl3+因形成沉淀而不能大量共存;
D. K-、H、CO、MnO2+
F. e2+与NO+(H)因发生氧化还原反应而不能大量共存;
H. +)因发生氧化还原反应而不能大量共存;
解析:【解析】
A. I-的还原性强于Fe
B. I2的氧化性强于Fe3+
C. ③易发生的主要原因是Fe(OH)3比Fe(OH)2更难溶
D. 溶液酸碱性对Fe3+和Fe2+的氧化性或还原性没有影响
解析:【解析】由①可知还原性:I->Fe2+,由②可知还原性:Fe>Fe2+,无法判断I-和Fe的还原性强弱,A项错误;由①可知氧化性:Fe3+>I2,B项错误;由③可知,碱性条件下I2能将Fe(OH)2氧化为Fe(OH)3,所以溶液酸碱性对Fe3+和Fe2+的氧化性或还原性有影响,D项错误。
A. H2O和H2O2是化合物,不是单质,故H2O和H2O2不属于同素异形体,故A错误;
B. O2和O3都是由氧元素形成的不同物质,都是单质,互为同素异形体,故B正确;
C. 金刚石和石墨都是由碳元素形成的不同物质,都是单质,互为同素异形体,故C正确;
D. 红磷和白磷都是由磷元素形成的不同物质,都是单质,互为同素异形体,故D正确。
解析:【解析】由同种元素形成的不同种单质互为同素异形体,互为同素异形体的物质要符合以下两个条件:同种元素形成,不同单质;据此进行分析判断.判断同素异形体的关键把握两点:①同种元素形成,②不同单质。
解析:【解析】在书写离子方程式时,碳酸钙、Fe2O3、单质铁、CO2、H2、H2O等用化学式表示。Ca(OH)2微溶于水,溶液(澄清石灰水)状态用离子符号表示,浊液(石灰乳)状态用化学式表示。
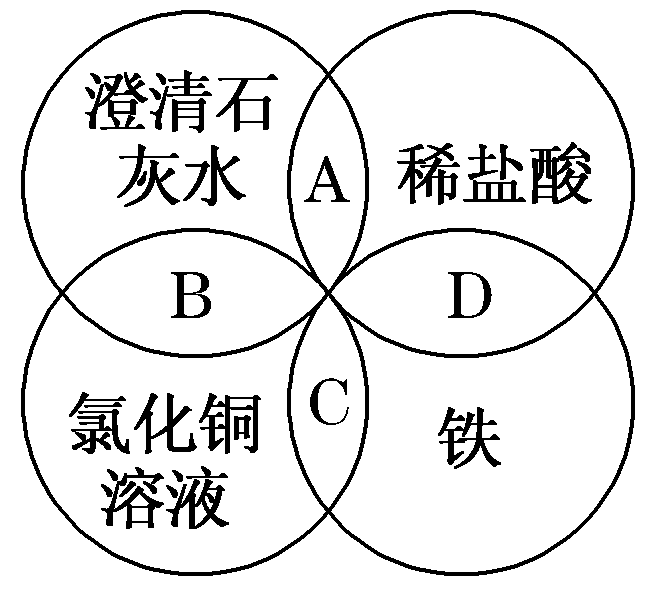
A. 项正确的离子方程式为OH-+H+===H2O;
B. 项正确的离子方程式为
C. u2++2OH-===Cu(OH)2↓;
D. 项正确的离子方程式为Fe+2H+===Fe2++H2↑。
F. e+2H+===Fe2++H2↑。
H. +===Fe2++H2↑。
解析:【解析】
A. 胆矾 CuSO4·5H2O 混合物
B. 氖气 Ne 单质
C. 烧碱 NaOH 氧化物
D. 纯碱 NaOH 碱
解析:【解析】胆矾是纯净物;烧碱不是氧化物;纯碱属于盐而不是碱。下列各组物质不属于同素异形体的是
A. 化合物电离时,生成的阳离子全部是氢离子的才是酸;
B. 化合物电离时,生成的阴离子全部是氢氧根离子的才是碱;
C. 稀硫酸
D. NH4Cl是盐,从化学性质上看,NH可看成金属阳离子。
解析:【解析】
A. Na2O2、MgO、Al2O3均属于碱性氧化物
B. 纯碱、烧碱、熟石灰均属于碱
C. 酸、碱、盐之间发生的反应均属于复分解反应
D. 混合物、分散系、胶体从属关系如图所示
解析:【解析】能与酸反应且只生成盐和水的氧化物称为碱性氧化物,所以Na2O2不属于碱性氧化物,Al2O3属于两性氧化物,故A错误;纯碱为Na2CO3,属于盐而不属于碱,故B错误;酸、碱、盐之间发生的反应并不都属于复分解反应,如硝酸跟氢氧化亚铁的反应,故C错误;胶体是分散系的一种,分散系都属于混合物,故D正确。
解析:【解析】(1)③铁中有自由电子,所以能导电,⑥熔融的K2SO4中有自由移动的离子,所以能导电;⑧石墨有自由电子,所以能导电,①碳酸氢钠晶体②液态氯化氢④蔗糖⑤酒精⑦干冰中没有自由移动的离子或自由电子,所以不能导电,故答案为:③⑥⑧;(2)在水溶液里和熔融状态下都不能导电的化合物是非电解质,④蔗糖⑤酒精⑦干冰属于非电解质,故答案为:④⑤⑦;(3)①碳酸氢钠晶体②液态氯化氢⑥熔融的K2SO4⑦干冰溶于水后,溶液中存在自由移动的离子而导电,故答案为:①②⑥⑦;(4)碳酸氢钠晶体与液态氯化氢在水溶液中反应生成氯化钠、二氧化碳和水,离子方程式为:H++HCO ═H2O+CO2↑;故答案为:NaHCO3═Na++HCO、K2SO4═2K++SO;(5)Ⅰ向溶液中加入过量的BaCl2溶液,有白色沉淀产生,过滤,则含SO、CO中的一种或都有,则一定没有Ba2+;Ⅱ向Ⅰ中滤液里加入AgNO3溶液,有白色沉淀产生,白色沉淀为AgCl,但Ⅰ引入氯离子,则不能确定是否含Cl−;Ⅲ将Ⅰ中的沉淀加入稀盐酸中,沉淀部分消失,有气体产生,则一定含SO、CO,则没有H+,因溶液不显电性,则一定含Na+,综上所述,一定含SO、CO、Na+,一定没有H+、Ba2+,可能含有Cl-;取少量溶液于试管中,向溶液中滴加硝酸酸化的AgNO3溶液,若产生白色沉淀,则证明原溶液中含有Cl-。故答案为:SO、CO、Na+;H+、Ba2+;Cl-;取少量溶液于试管中,向溶液中滴加硝酸酸化的AgNO3溶液,若产生白色沉淀,则证明原溶液中含有Cl-。