

A、 项正确的离子方程式为OH-+H+===H2O;
B、 项正确的离子方程式为
C、 u2++2OH-===Cu(OH)2↓;
D、 项正确的离子方程式为Fe+2H+===Fe2++H2↑。
F、 e+2H+===Fe2++H2↑。
H、 +===Fe2++H2↑。
答案:C
解析:【解析】



A、 项正确的离子方程式为OH-+H+===H2O;
B、 项正确的离子方程式为
C、 u2++2OH-===Cu(OH)2↓;
D、 项正确的离子方程式为Fe+2H+===Fe2++H2↑。
F、 e+2H+===Fe2++H2↑。
H、 +===Fe2++H2↑。
答案:C
解析:【解析】



A. 由于受热均易分解,而湿度大会使纸张变质,保存该画需控制温度和湿度,故A不选;
B. 均不能被空气氧化,故B不选;
C. 均易与酸反应,不耐酸,故C可选;
D. 由于中铜元素质量分数高于中铜元素质量分数,所以中铜元素质量分数高于,故D不选。
解析:【解析】
A. Cu 和SO4
和SO4
B. Cu2+和Cl2+
C. K 和SO2+
和SO2+
D. Ag和NO+
解析:【解析】Cu2++2OH-=Cu(OH)2↓,Ba2++SO =BaSO4↓。
=BaSO4↓。
A. NaOH溶液和CO2的反应
B. Ba(OH)2溶液和稀H2SO4的反应
C. NaOH溶液和盐酸的反应
D. 氨水和稀H2SO4的反应
解析:【解析】只有可溶性的强酸与可溶性的强碱反应生成可溶性的盐和水的反应才符合条件。
A. ①②③④
B. ②③④
C. ①③④
D. ①②③
解析:【解析】①铜与氧气反应生成氧化铜,氧化铜与硫酸反应生成硫酸铜,硫酸铜与硝酸钡反应生成硝酸铜,铜和浓硫酸反应可生成硫酸铜,再利用较活泼金属与不活泼金属的盐溶液发生的置换反应可实现丙→甲、丁→甲的反应,故①能实现转化。②碳酸钠和氢氧化钙反应生成氢氧化钠,氢氧化钠和二氧化碳反应生成碳酸氢钠,碳酸氢钠分解或与盐酸反应生成二氧化碳,二氧化碳与氢氧化钠能反应生成碳酸钠,碳酸钠与二氧化碳反应生成碳酸氢钠,碳酸氢钠与氢氧化钠反应生成碳酸钠,故②能实现转化。③(NH4)2SO3和氯化钙反应生成亚硫酸钙沉淀,亚硫酸钙和盐酸反应生成二氧化硫,过量的二氧化硫和一水合氨反应生成亚硫酸氢铵,故③能实现转化。④Fe与水蒸气在高温下反应生成Fe3O4,Fe3O4被还原可生成FeO,FeO可与盐酸反应生成FeCl2,FeCl2可被置换生成Fe,Fe在高温下与氧气反应生成FeO,FeO可与CO反应生成Fe,故④能实现转化。
A. HCl→H2
B. CO2→CO
C. FeCl3→FeCl2
D. SO2→SO3
解析:【解析】需要加入合适的氧化剂,则上述变化发生氧化反应,化合价升高,所以D选项正确。
A. 银与稀硫酸不反应;
B. 稀硫酸与氢氧化钡溶液混合:2H3+SO2+Ba3+2OH+=BaSO3+↓+2H2O;
C. 稀硝酸滴在大理石上:CaCO++2H+=Ca++H2O+CO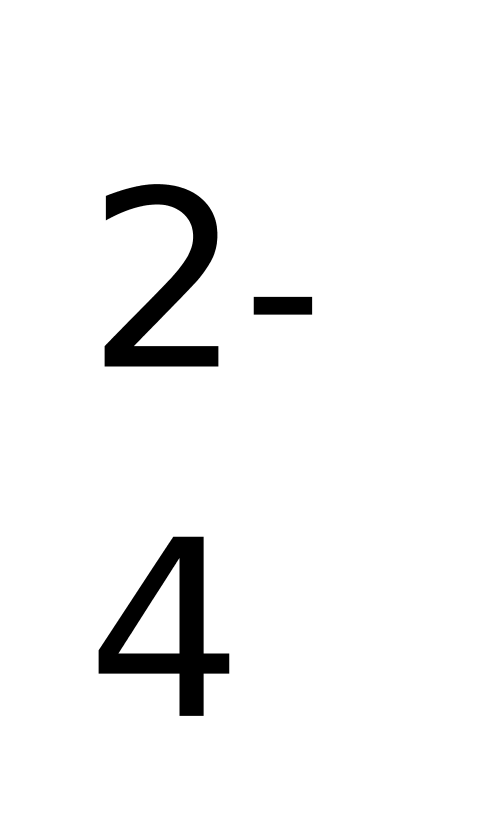 ↑。
↑。
D. 氧化铁与稀盐酸混合:Fe2+O4+6H3=2Fe++3H2+O
解析:【解析】
A. K-、Na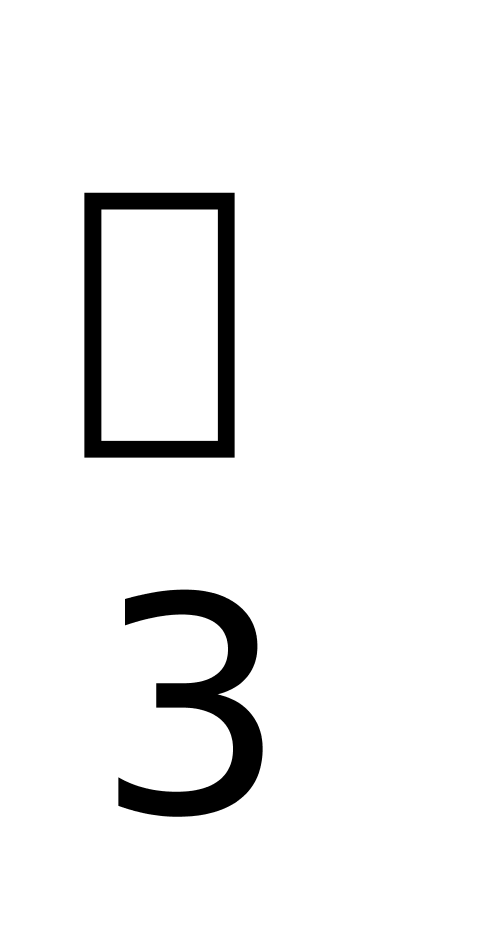 、Cl+、NO2+ - ++-
、Cl+、NO2+ - ++-
B. Cu、NO、OH、HCO
C. Na、OH2+、Cl 、NO-
、NO- +2+ - +
+2+ - +
D. OH+、K-、S 、Na
、Na
解析:【解析】B 中 Cu2+ 有颜色,且不能与 OH- 共存。
A. 豆浆
B. 蔗糖溶液
C. 牛奶
D. 烟、云、雾
解析:【解析】只有胶体才能发生丁达尔效应,ACD选项均为胶体,B选项为溶液,所以选B。
A. 由于受热均易分解,而湿度大会使纸张变质,保存该画需控制温度和湿度,故A不选;
B. 均不能被空气氧化,故B不选;
C. 均易与酸反应,不耐酸,故C可选;
D. 由于中铜元素质量分数高于中铜元素质量分数,所以中铜元素质量分数高于,故D不选。
解析:【解析】
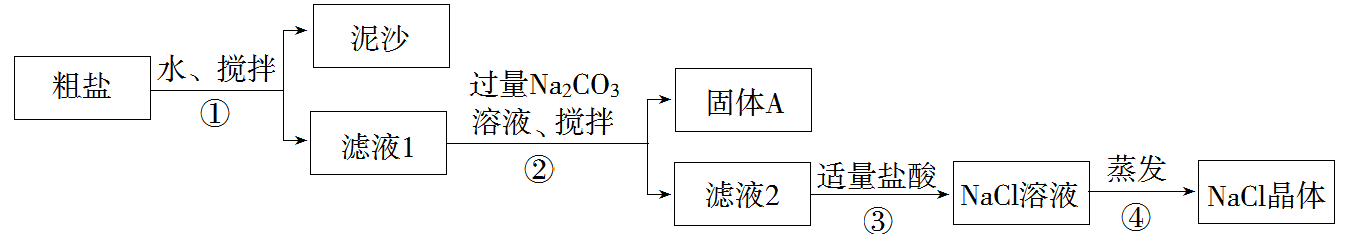 (1)步骤①和②的操作名称是()()。(2)步骤③判断加入盐酸“适量”的方法是()()()。步骤④加热蒸发时要用玻璃棒不断搅拌,这是为了防止()(),当蒸发皿中有较多量固体出现时,应()(),用余热使水分蒸干。(3)猜想和验证:
(1)步骤①和②的操作名称是()()。(2)步骤③判断加入盐酸“适量”的方法是()()()。步骤④加热蒸发时要用玻璃棒不断搅拌,这是为了防止()(),当蒸发皿中有较多量固体出现时,应()(),用余热使水分蒸干。(3)猜想和验证:
解析:【解析】(1)粗盐提纯步骤为溶解、过滤、蒸发结晶,步骤①和②是将固体和液体分离,操作方法都是过滤;(2)滤液2中有过量的Na2CO3,加入盐酸时产生气泡,当滴加盐酸至刚好无气泡放出时说明恰好完全反应,此时盐酸的量为适量。(3)取少量固体A于试管中,滴加稀盐酸,并用涂有澄清石灰水的小烧杯罩在试管口上方,如有气泡放出,澄清石灰水变浑浊,说明猜想Ⅰ成立;加入稀硝酸(或稀盐酸)有气泡放出,说明有CO3-放,再加Na2SO4溶液无白色沉淀,说明猜想Ⅱ不成立;在制得的NaCl溶液中滴入BaCl2溶液和稀硝酸,若有白色沉淀生成且不溶于稀硝酸,说明最后制得的NaCl晶体中含有Na2SO4,则猜想Ⅲ成立。